«Широко простирает химия руки свои в дела человеческие», — эта крылатая
фраза Михаила Ломоносова в настоящее время особенно актуальна.
Химия
сегодня — это продукты и лекарства, горючее и одежда, удобрения и
краски, анализ и синтез, организация производства и контроль качества
его продукции, подготовка питьевой воды и обезвреживание стоков,
экологический мониторинг и создание безопасной среды обитания человека.
«Овладеть таким объемом знаний невозможно!» — воскликнет пессимист.
«Ничего
невозможного нет для человека, увлеченного своим делом,»- отвечаем мы.
И
если вы химик или просто человек, увлеченный этой удивительной наукой,
мы ждем вас на нашем сайте.
Здесь вы узнаете о красивых цветных и
ярких химических реакциях с выделением дыма, выпадением осадка,
изменением цвета раствора, научитесь решать расчетные химические любой
сложности, сможете удалить ржавчину, жирное пятно, пятно от чая,
йода, крови, распознать подделку настоящих духов, туалетной воды и
многое другое.
Если Вы любите химию так, как любим ее мы, заходите на сайт, здесь вы найдете много полезного и интересного.
7 «Широко распространяет химия руки свои в дела человеческие… Куда ни посмотрим, куда ни оглянемся, везде обращаются пред очами нашими успехи ее прилежания». Приведите примеры, подтверждающие эти слова, и охарактеризуйте роль химии в современном мире. Докажите, что каждому человеку в наше время необходимо знать основы химии, «…которая ничего иного от вас не пожелает, как прилежного в ней упражнения, к вашему самих вас украшению и обогащению» (М. В. Ломоносов).
Абсолютное большинство предметов (бумага, банки, ручки, одежда, техника и др.), которыми мы пользуемся в повседневной жизни сделаны с использованием химии.
См. §1, ответ на на вопрос 1.
Материал из Викицитатника
Перейти к навигации
Перейти к поиску
Хи́мия (от араб. کيمياء, произошедшего, предположительно, от египетского слова km.t (чёрный), откуда возникло также название Египта, чернозёма и свинца — «черная земля»; другие возможные варианты: др.-греч. χυμος — «сок», «эссенция», «влага», «вкус», др.-греч. χυμα — «сплав (металлов)», «литье», «поток», др.-греч. χυμευσις — «смешивание») — одна из важнейших и обширных областей естествознания, наука о веществах, их свойствах, строении и превращениях, происходящих в результате химических реакций, а также законах, которым эти превращения подчиняются.
Химия в научной и научно-популярной литературе[править]
| | Мы сказали, что химическая наука рассматривает качества и изменения тел. Качества бывают двоякого рода, а именно, одни возбуждают у нас точно различимое представление, другие — только ясное. Первого рода качества — масса, фигура, движение или покой и местоположение каждого ощутимого тела; второго рода — цвет, вкус, целебные силы, сцепление частей и т. д. Первые и воспринимаются взором и определяются геометрическими и механическими законами, предметом которых они являются; причина же последних лежит в частях, недоступных остроте зрения, потому сами качества не могут быть определены геометрически и механически без помощи физической химии. Первые по необходимости присущи всем телам, вторые — только некоторым. Поэтому мы считаем целесообразным по почину Бойля называть первые качества — общими, вторые — частными. |
| — Михаил Ломоносов, Введение в истинную физическую химию, § 4, 1752 |
| | Химия сама создаёт свой объект. Эта творческая способность, сходная с творческой силой искусства, существенным образом отличает её от естественных и исторических наук.[1] |
| — Марселен Бертло (из книги «Химическая механика»). |
| | Химия существовала издавна в виде металлургии, то есть чисто прикладного умения добывать чистые металлы из руд и сплавов. Свое название (chemia, по-египетски «чернокнижие») она получила, однако, не от этой техники, а от темной практики египтян, которые как раз в нашу эпоху бились над задачей подделывать золото. Наружу они всплывают лишь в эпоху империи; тогда мы и займемся этой наукой.[2] |
| — Фаддей Зелинский, «История античной культуры», 1914 |
| | И далее, подобно тому, как 40 лет тому назад молодая физическая химия боролась за признание своей равноценности и самостоятельности наряду с наиболее старыми дисциплинами ― неорганической и органической химией, и ныне биологическая химия, химия коллоидов, все более и более расширяется в новую самостоятельную область знания и, как метко указал в своей речи в Германской Академии Наук Haber и, как отметил недавно в своем докладе в Вюрцбурге Willstätter, преобладание биохимических методов в органической химии является насущною потребностью дня, ибо стремление химика состоит в том, чтобы понять те пути, по которым протекают химические процессы в самой природе, которая часто, не знает тех насильственных путей ― высоких давлений и других сложных вспомогательных средств, которыми пользуется химик в своей лаборатории.[3] |
| — Макс Блох, «Пути современной химии», 1923 |
Химия в публицистике и художественной прозе[править]
| | Широко распростирает химия руки свои в дела человеческие… Куда ни посмотрим, куда ни оглянемся — везде обращаются перед очами нашими успехи её прилежания. |
| — М. В. Ломоносов |
| | Не такой требуется математик, который только в трудных выкладках искусен, но который, в изобретениях и в доказательствах привыкнув к математической строгости, в натуре сокровенную правду точным и непоползновенным порядком вывесть умеет. Бесполезны тому очи, кто желает видеть внутренность вещи, лишаясь рук к отверстию оной. Бесполезны тому руки, кто к рассмотрению открытых вещей очей не имеет. Химия руками, математика очами физическими по справедливости назваться может.[4] |
| — Михаил Ломоносов, Слово о пользе химии, 1751 |
| | — Да, я химик, — сказал Санька, едва отрываясь от затасканных иллюстраций. |
| — Борис Житков, «Виктор Вавич», 1934 |
| | В физике, как известно, «капризов» практически нет, в то же время биология полна ими. Химия занимает промежуточное положение: иногда <химическая> реакция течет нормально, а иногда — сплошные «капризы». Цепная теория — это «теория капризов» химического превращения… |
| — Николай Семёнов, из „нобелевского“ интервью газете «Правда», 1956 |
| | А для меня он давным-давно стерся и растворился в маленьком ручейке школьного полузнания загадочной и тогда мне совсем неинтересной науки, о которой сохранилась в памяти только дурацкая школярская припевка: «Химия, химия ― вся макушка синяя».[6] |
| — Аркадий Вайнер, Георгий Вайнер. «Лекарство против страха», 1987 |
| | Но опять-таки вспомним о достижениях химии. Бандера ― синильная кислота, Хохлов ― радиоактивный барий, зонтик, убивший болгарина Георгия Маркова, был заряжен пулей, отравленной веществом, называемым рицин. А еще была серия непонятных ожогов, от которых пострадали Александр Солженицын, французский профессор Жорж Нива, в Москве ― еврейский отказник Лев Рубинштейн, в Ленинграде ― Илья Левин. Ожоги загадочные, а кто это сделал?[7] |
| — Владимир Войнович, «Дело № 34840», 1999 |
| | Кто-то напрягается с тостами, буреет, старается провести мероприятие на уровне. Помню, как Константин Федин закричал: «И это аквамариновое море!..» ― о только что построенном бассейне «Москва». Дальше сплошняком пошла химия. Химия, химия. Химия тут, химия там… Вплоть до того, что все имеющееся на столе сможет сотворить химия. Хрущев хохотнул и сказал: |
| — Нонна Мордюкова, «Казачка», 2005 |
Химия в поэзии[править]
| | Сосед мой химик, симпатичный малый, |
| — Саша Чёрный, «Химические стихи», 1928 |
| | История мучит людей, |
| — Борис Слуцкий, «История мучит людей…», 1975 |
Источники[править]
- ↑ Вальден П.К., «Марселен Бертло». Рига, 1913. стр. 11.
- ↑ Зелинский Ф.Ф. «История античной культуры». — СПб.: Марс, 1995 г.
- ↑ Макс Блох. Пути современной химии. — М.: «Природа», № 1-6, 1923 г.
- ↑ М. В. Ломоносов. «Избранные философские произведения» //Госполитиздат, Москва, 1950 г. — с.172.
- ↑ Житков Борис. «Виктор Вавич»: Роман / Предисл. М. Поздняева; Послесл. А. Арьева. — М.: Издательство Независимая Газета, 1999 г.
- ↑ Аркадий Вайнер, Георгий Вайнер. «Лекарство против страха». — Москва: Советский писатель, 1986 г.
- ↑ Войнович В. Замысел. — М.: Вагриус, 2000 г.
- ↑ Берлин А. Идеи, теории и полимеры // Наука и жизнь. — 2019. — № 10. — С. 28.
- ↑ Нонна Мордюкова. Казачка. — М.: Вагриус, 2005 г.
- ↑ Саша Чёрный, собрание сочинений в пяти томах, — Москва: «Эллис-Лак», 2007 г.
- ↑ Б.А.Слуцкий. Собрание сочинений: В трёх томах. — М.: Художественная литература, 1991 г.
См. также[править]
- Физика
- Физическая химия
- Химическая физика
- Минералогия
Игра-конкурс «Широко распростирает химия руки свои в дела человеческие»
( М.В. Ломоносов).
Станция «Менделеевцы»
8 класс. Учитель: Здравствуйте, дорогие ребята! Сегодня мы определим самого умного химика школы. Для этого наши участники пройдут испытания в виде конкурсов. За каждый правильный ответ они будут получать по жетону. В конце игры будут подводиться итоги.
Сначала мы попросим представиться участников. Учитель: Вам будут задаваться вопросы. Кто первый ответит, получает жетон. Ответ принимается только у участника с поднятой рукой. Если участники выкрикивают, вопрос ни кому не засчитывается. Учитель: Вам будут задаваться вопросы. Кто первый ответит, получает жетон. Ответ принимается только у участника с поднятой рукой. Если участники выкрикивают, вопрос ни кому не засчитывается.
И так мы начинаем! Желаем всем участникам « Ни пуха , ни пера…..
Конкурс 1.
-
Разгадайте загадки.
-
Что видно, когда ничего не видно? ( туман)
-
Темным облаком летела,
Опустилась птицей белой,
Превратилась в человечка,
Постояла у крылечка,
Покатилась кувырком
И запела ручейком. (вода)
-
На дворе переполох-
С неба сыплется горох,
Съела шесть горошин Нина-
У нее теперь ангина. ( град )
-
Без пути и без дороги
Ходит самый длинноногий.
В тучах прячется, во мгле,
Только ноги на Земле. ( дождь)
-
Без крыльев летят,
Без ног бегут,
Без паруса плывут. ( облака)
-
Не снег и не лед, а серебром
Деревья уберет ( иней)
-
Это газ, необходимый растениям для фотосинтеза. ( углекислый газ)
-
Прославлен всеми письменами
Металл, испытанный огнем.
Манил к себе людей веками,
Алхимик жил в мечтах о нем.
В средневековье феодалы
Войною шли из-за него
И королевские подвалы
Хранили слитками его. ( золото)
-
Викторина.
-
Назовите восемь наименований состояния воды, принятых в метеорологии.
( пар, лед, туман, облака, иней, град, тучи, снег).
-
Можно ли высушить белье на морозе? ( можно, т.к. лед тоже испаряется).
-
Почему яйцо не тонет в соленой воде? ( потому что плотность соленой воды больше, чем пресной, значит, больше и выталкивающая сила).
Станция «Менделеевцы».
9 класс
Учитель: Здравствуйте, дорогие ребята! Сегодня мы определим самого умного химика школы. Для этого наши участники пройдут испытания в виде конкурсов. За каждый правильный ответ они будут получать по жетону. В конце игры будут подводиться итоги.
Сначала мы попросим представиться участников. Учитель: Вам будут задаваться вопросы. Кто первый ответит, получает жетон. Ответ принимается только у участника с поднятой рукой. Если участники выкрикивают, вопрос ни кому не засчитывается.
И так мы начинаем! Желаем всем участникам « Ни пуха , ни пера…..
Конкурс 1. «Разминка»
-
Название какого химического элемента слагается из названия двух животных? (мышьяк)
-
Без какого элемента невозможна фотография? ( серебро)
-
Какой металл самый легкий? ( литий)
-
Мельчайшая частица , химически не делимая? ( атом)
-
Самый распространенный химический элемент на Земле?
( кислород)
-
Какой металл называют элементом плодородия? ( калий)
-
Какие элементы образуют простые вещества, находящиеся в жидком состоянии? ( ртуть и бром)
-
Самый распространенный химический элемент во Вселенной?
( гелий)
-
Какой самый тугоплавкий металл? ( вольфрам)
Конкурс 2 « Угадай элемент»
-
Есть в языке нашем чудное слово
И четверо школьников спорят о нем.
Младший сказал: «Это лес. Только хвойный»,
Второй возразил: «Элемент так зовут».
Третий воскликнул без тени сомненья:
«Это, друзья, инструмент для сверленья:
Тут молвил четвертый: «Секрета здесь нет,
Эту фамилию знает весь свет».
И все четверо были правы. Что это за слово? ( Бор)
•Прославлен всеми письменами
Металл, испытанный огнем.
Манил к себе людей веками,
Алхимик жил в мечтах о нем.
В средневековье феодалы
Войною шли из-за него
И королевские подвалы
Хранили слитками его. ( золото)
-
Хранят обычно в керосине, и «бегает» он по воде.
В природе, помните отныне,
Свободным нет его нигде.
В солях открыть его возможно,
Желтеет пламя от него,
И получить из соли можно
Как Дэви получил его. ( натрий)
-
Давно известна человеку,
Она тягуча и красна.
Еще по «бронзовому веку»
Знакома в сплавах всем она.
С горячей серной кислотою
Дает нам синий купорос.
Так что же это за металл?
Ответьте на вопрос. ( Медь)
-
Среди металлов самый славный,
Важнейший древний элемент.
В тяжелой индустрии главный,
Знаком с ним каждый человек.
Родится в огненной стихии,
Расплав его течет рекой,
Важнее нет в металлургии,
Он нужен всем, и нам с тобой. ( железо)
-
Был металл серебристо-белый,
В соединении стал мелом. ( кальций)
Конкур « Угадай явление»
Опыт « Вулкан»
Назовите признаки реакции.
Вы можете ознакомиться и скачать
«Широко распростирает химия руки свои в дела человеческие! «Широко распростирает химия руки свои в дела человеческие! Куда ни.
Презентация содержит 26 слайдов.
Презентации для любого
класса можно скачать бесплатно. Если материал и наш сайт презентаций Вам
понравились
–
поделитесь им с друзьями с помощью социальных кнопок и добавьте в закладки в
своем
браузере.
Слайды и текст этой презентации
Слайд 1
Описание слайда:
«Широко распростирает химия руки свои в дела человеческие!
«Широко распростирает химия руки свои в дела человеческие!
Куда ни посмотрим, куда ни оглянемся, везде обращаются пред очами нашими успехи ее прилежания.»
М.В.Ломоносов
Слайд 2
Описание слайда:
О чем пойдет речь сегодня на уроке?
ЧТО ИХ ОБЪЕДИНЯЕТ?
Слайд 3
Описание слайда:
СПИРТЫ
СПИРТЫ
(аканолы, алкоголи)
Слайд 4
Описание слайда:
Цель:
Сформировать знания о новом классе органических веществ: спиртах.
Слайд 5
Описание слайда:
План действий:
— Рассмотреть строение спиртов.
— Выяснить классификацию спиртов.
— Научиться называть спирты.
— Рассмотреть изомерию спиртов.
— Выяснить какие физические свойства характерны для спиртов.
— Разобрать физиологическое влияние спиртов на организм человека.
Слайд 6
Описание слайда:
Задания по группам:
— 1-я группа: разобрать строение спиртов.
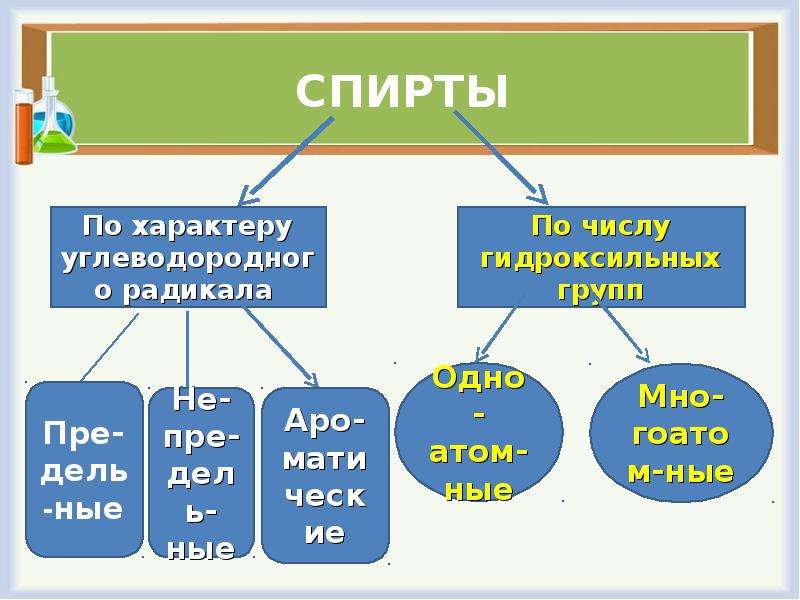
— 2-я группа: изучить классификацию спиртов.
— 3-я группа: рассмотреть номенклатуру спиртов.
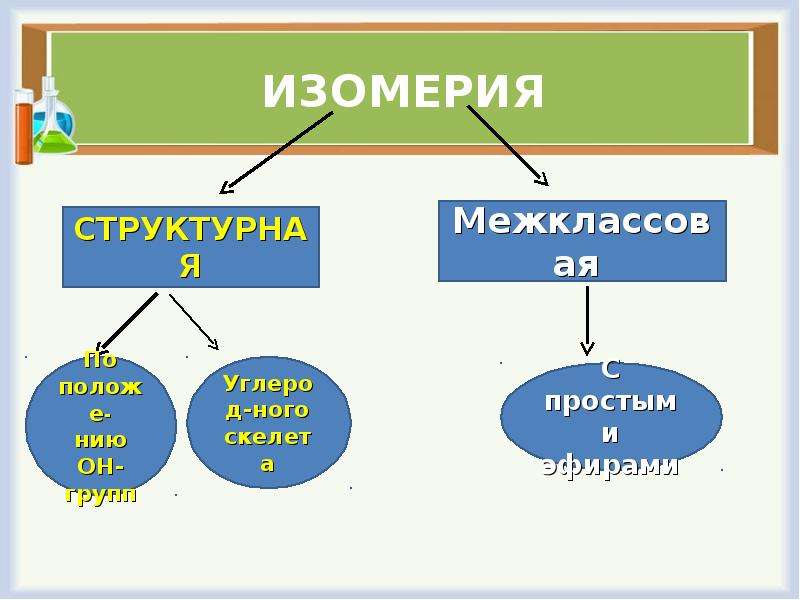
— 4-я группа: рассмотреть изомерию спиртов.
Слайд 7
Описание слайда:
Организация работы:
Группа:
Работает над своим вопросом;
Готовит ответ у доски по своему вопросу (время – 5минут);
Внимательно слушает объяснение других групп;
Делает записи в тетради;
Участвует в обсуждении ответа других групп.
Слайд 8
Описание слайда:
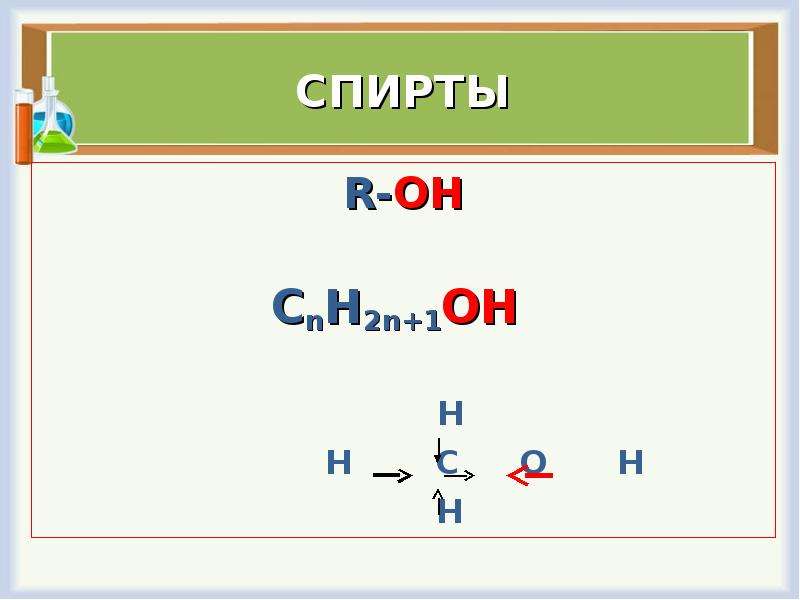
СПИРТЫ
R-OH
СnH2n+1OH
H
H C O H
H
Слайд 9
Слайд 10
Описание слайда:
Закрепим:
Определите к какому виду спиртов относятся вещества:
а) C3H7OH б)CH3-CH=CH-CH2-OH
в) CH3-CH-CH2-CH-CH3
ОН ОН
г) CH2-CH2-OH
C6H5
Слайд 11
Описание слайда:
НОМЕНКЛАТУРА
УГЛЕВОДОРОД + ОЛ
УГЛЕВОДОРОД + ОЛ + цифра
УГЛЕВОДОРОД + приставки (ди, три т. д.) ОЛ + цифра
Слайд 12
Описание слайда:
Назовите спирты:
CH3-CH2-CH2-OH
CH3-CH2-CH-CH2-CH3
ОН
CH2-CH2- CH2-CH2
ОН ОН
Слайд 13
Описание слайда:
ИЗОМЕРИЯ
Слайд 14
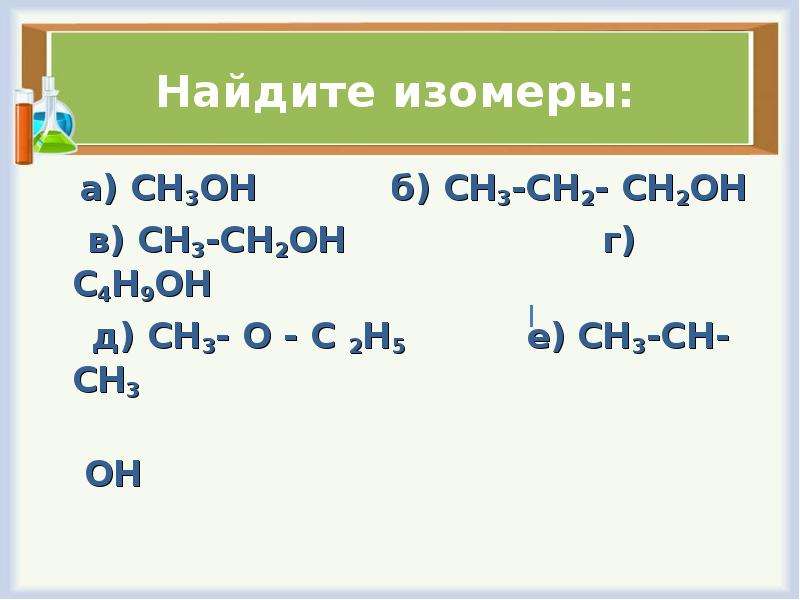
Описание слайда:
Найдите изомеры:
а) CH3OH б) CH3-CH2- CH2OH
в) CH3-CH2OH г) C4H9OH
д) CH3- O — C 2H5 е) CH3-CH-CH3
ОН
Слайд 15
Описание слайда:
Исследование физических свойств спиртов:
Изучите и опишите физические свойства этанола и пропанола-1
Слайд 16
Описание слайда:
проблема
Почему спирты растворяются в воде,
в отличие от углеводородов?
Слайд 17
Описание слайда:
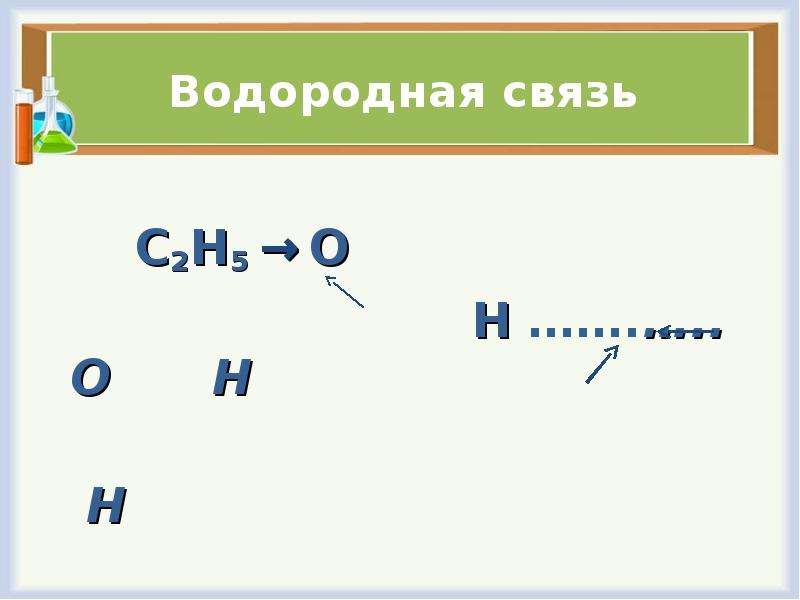
Водородная связь
С2Н5 → О
Н …….….. О Н
Н
Слайд 18
Описание слайда:
Спирт и опиум – близнецы ада и гибели.
Эдгард По
Слайд 19
Слайд 20
Слайд 21
Описание слайда:
Урок результативный
если Вы:
Знаете строение предельных спиртов.
Умеете давать определение спиртам, классифицировать спирты, называть спирты.
Объясняете физические свойства спиртов.
Слайд 22
Описание слайда:
Первичное закрепление:
1. Общая формула предельных одноатомных спиртов:
а) СnH2n(ОН)2 б) СnH2n+1ОН в) R(ОН)n г) СnH2nСОН
2. Назовите соединение СН3─СН─СН2─СН2ОН
|
СН3
а) 3-метилбутанол-1 б) 2-метилбутанол-4
3. Укажите тип изомерии предельных одноатомных спиртов:
а) углеродные цепи б) положение ОН-группы
в) цистрансизомерия г) межклассовая
4. Формула спирта:
а) СН3─СН2─СН2ОН б) СН3─СН2─СОН в) СН3─СО ─СН3
5. Гомологом для этанола является:
а) этаналь б) этановая кислота в) этандиол г) метанол
Слайд 23
Описание слайда:
ЭТАЛОН:
1. б
2. а
3. абг
4. а
5. г
Слайд 24
Описание слайда:
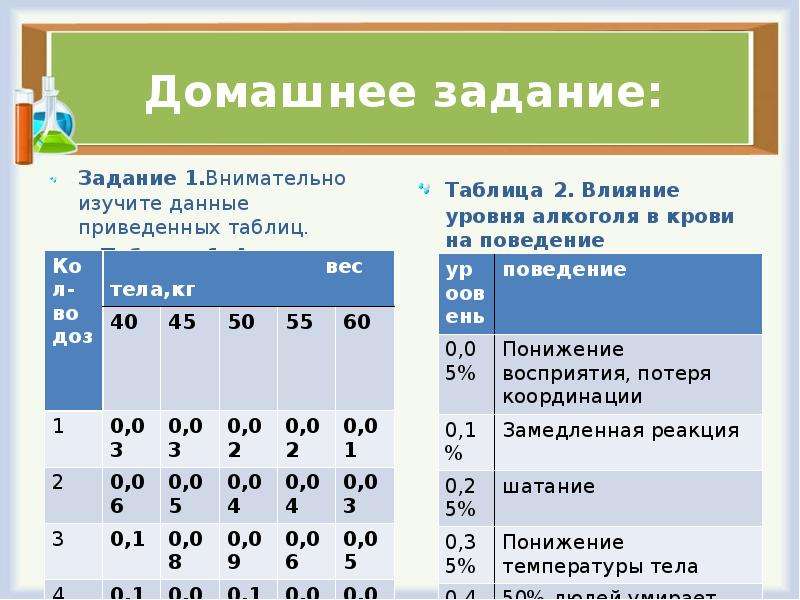
Домашнее задание:
Задание 1.Внимательно изучите данные приведенных таблиц.
Таблица 1. Алкоголь в крови.
Слайд 25
Описание слайда:
Используя информацию таблиц,ответить на вопросы:
1группа: Если человек весом 50 кг выпьет бутылку вина, какое содержание спирта у него будет ?
2 группа: Если человек весом 55 кг выпьет подряд 6 стаканов вина, а через час сядет за руль, может ли это привести в ДТП?
3 группа: Если человек весом 40 кг выпьет 8 рюмок водки, возникает ли опасность для его жизни?
4 группа: Сколько времени должен не садиться за руль автомобиля человек весом 60 кг, выпивший 3 бутылки пива?
Слайд 26
Описание слайда:
Оцените свою работу на уроке:
Работа в группе:
работал по учебнику – 1б
отвечал у доски – до 3 б ( ответ совпал с эталоном – 3б, в ответе есть- неточности – 2б, много неточностей – 1б)
участвовал в обсуждении других вопросов – до 3 б ( активно – 3б, иногда — 2б, редко -1б)
2. Работа в паре — до 3 б ( был организатором работы – 3 б, исполнителем – 2 б, слушателем – 1б)
3. Тест :
5 правильных ответов – 5 б
4 правильных ответа – 4 б
3 и меньше – 1 б
Если вы набрали –13 – 12 баллов – «5»
11- 9 баллов – «4»
8 и меньше –дома нужно поработать!
«Все испытал и все проник» — писал о М.В. Ломоносове А.С.Пушкин.
Одной из целей данной конференции —
— воспитание убежденности в возможности познания законов природы и использование достижений науки на благо развития человеческой цивилизации
19 ноября – это день рождения М.В.Ломоносова гениального русского ученого, трудами которого в России был заложен фундамент различных отраслей науки и техники.
Что же он испытал и во что проник – маленький обзор.
М.В.Ломоносов жил в эпоху, когда химия только зарождалась как наука и тем не менее он смог наперекор представлениям флогистонской теории дойти до таких обобщений, которые и сегодня лежат в основе физической и химической науки.
М.В. Ломоносов – создатель первой в России
химической лаборатории. Ученый имел отчетливое
представление о химически чистом веществе и реактиве,
о чем почти не помышляли западные химики и отчего
происходила постоянная путаница в опытах. Лаборатория
Ломоносова располагала целым набором различных
весов. Здесь он производил анализы минералов и
образцов руд, присылаемых со всех концов России.
М.В. Ломоносов был создателем
многих химических производств
(неорганических пигментов,
глазурей, стекла, фарфора). Он
разработал технологию и
рецептуру цветных стекол, которые
употреблял для создания
мозаичных картин; изобрел фарфоровую массу. Учёный занимался
анализом руд, солей и других продуктов. В труде “Первые
основания металлургии, или рудных дел” он рассмотрел свойства
различных металлов, дал их классификацию и описал способы
получения.
Доказывал органическое происхождение нефти, каменного угля, торфа и
янтаря. Им описаны процессы получения железного купороса,
меди из медного купороса, серы из серных руд, квасцов, серной,
азотной и соляной кислот. Ломоносов обратил внимание на
основополагающее значение закона сохранения массы вещества
в химических реакциях; изложил основы своего
корпускулярного (атомно-молекулярного) учения, получившего
развитие лишь спустя столетие; выдвинул кинетическую теорию
теплоты; обосновал необходимость привлечения физики для объяснения химических
явлений и предложил для теоретической части химии название “физическая химия”, которая существует и поныне, а для
практической части -“техническая химия”. Он впервые высказал мнение о том, что тела
состоят из “корпускул”, а те в свою очередь из “элементов”. В своём знаменитом “Слове о
пользе химии” Ломоносов ещё раз подчеркнул, что для успеха химической науки “требуется
весьма искусный химик и глубокий математик в одном человеке…“.
Ученый создал различные приборы (вискозиметр, прибор для
фильтрования под вакуумом, прибор для определения твердости, газовый
барометр, пирометр, котел для исследования веществ при низком и высоком
давлениях), достаточно точно градуировал термометры. Одним из
конкретных проявлений всеобщего закона природы был открытый и
экспериментально подтвержденный Ломоносовым закон сохранения
вещества при химических превращениях, установление которого
приписывалось французскому химику Антуану Лорану Лавуазье.
Труды Ломоносова в области физики явились крупным вкладом в эту важнейшую науку о природе. Они развивались и дополнялись учеными последующих лет и способствовали тому, что физика стала общепризнанным лидером естествознания.
Ломоносов в астрономии открыл атмосферу Венеры и этот приоритет открытия никем не оспаривается
В области геологии и минералогии была четко сформулирована теория эволюции, лежащая в основе всех явлений природы. Ломоносов изучал причины и природные последствия сейсмических катастроф. Ломоносов ввел в русский язык такие слова, как атмосфера, горный хребет, земная ось, удельный вес и др.
Он подготовил и отредактировал Минеральный каталог Кунсткамеры Академии наук, который был опубликован в 1745году и содержал более трех тысяч образцов руд и минералов.
Один из минералов, найденный в горной породе российские ученые назвали в честь своего великого предшественника ломоносовитом
Ломоносов увлекался и изучал математику, ботанику, историю России, произвел реформу в области русского языка и литературы, утвердил систему русского стихосложения
Во второй половине 18 века русскими мореплавателями была предпринята попытка проникнуть вглубь Северного Ледовитого океана, достичь полюса и пройти в Тихий океан. Эта экспедиция была организована по инициативе М.В.Ломоносова, который, основываясь на опыте русских поморов, пришел к выводу о возможности плавания Северным морским путем . Еще одно открытие: изучая процесс образования морского льда в «Сибирском океане» , Ломоносов установил, что температура замерзания морской воды зависит от ее солености.
М.В.Ломоносов приложил немало сил и в создании картографии России. Научное картографирование в России связано с деятельностью Географического депортамента
Академии Наук, который в 1758г. возглавил М.В.Ломоносов. Он собрал сведения о природе и экономике губерний, провинций, каждого поселения. Всего Географический департамент изготовил свыше 250 карт и планов.
Ломоносов – художник и химик он обратил внимание на мозаику- древнее искусство составлять из цветных стеклянных сплавов (смальт) немеркнущие картины и портреты . И об этих его мозаичных работах вы услышите из следующих выступлений.
«Широко распростирает химия
руки свои в дела человеческие»
М.В. Ломоносов
Одна из задач нашей конференции – применение научных знаний в приобретаемой профессии. А наши профессии – это повар-кондитер.
И сегодня мы остановимся на Пищевых добавках.
В нашей стране список разрешенных пищевых добавок значительно меньше чем за рубежом. Индекс Е специалисты отождествляют как
со словом «Европа» так и со словом «Съедобный»
Присвоение конкретному веществу статуса пищевой добавки и трехзначного номера с индексом «Е» подразумевает, что данное вещество проверено на безопасность.
Однако всегда есть риск, чтотнекоторые люди, например астматики, аллергики и маленькие дети, могут пострадать от пищи, содержащей пищевые добавки.
Согласно Европейской цифровой классификации пищевые добавки подразделяются следующим образом:
Е100 – Е182 — красители (усиливают или восстанавливают цвет продукта);
Е200 – Е299 — консерванты (повышают срок хранения продуктов, защищая от микробов и грибков; химические стерилизующие добавки при созревании вин);
Е300 — Е399 — антиокислители (защищают пищевые продукты от окисления, например жиры от прогоркания, и изменения цвета)
Е400 – Е499 — эмульгаторы (создают однородную смесь несмешиваемых составных частей пищи. Например воды и масла)
Е500 – Е599 — регуляторы кислотности
Е600 – Е699 — усилители вкуса и аромата
Е700 – Е800 — запасные индексы для другой информации
Е900 – и далее – улучшители вкуса хлеба, пеногасители, предупреждают или снижают образование пены в некоторых продуктах питания.
Консерванты – это вещества, которые добавляются в пищевые продукты для максимального их сохранения, предотвращения их порчи.
При выборе консервантов учитывается то, что они не должны иметь токсических и экологических последствий. В продуктах повседневного потребления (хлеб, молоко, сливочное масло) применение консервантов нежелательно.
Бензойная кислота (Е210) входит в состав некоторых ягод – брусники, клюквы и является распространенным природным консервантом.
Прменяется бензойная кислота при изготовлении плодово-ягодных изделий, соли бензойной кислоты – бензоаты – в производстве рыбных консервов,
маргаринов, напитков. О
Пропионовая кислота (Е280) — СН – СН – С
И ее соли натрия , калия и кальция применяют в сыроделии, хлебопечении но применение их ограничено ввиду неприятного запаха.
Чаще применяют сорбиновую кислоту (Е200) и ее соли в производстве сыров всех видов, молочных и кисло-молочных продуктов, хлебопечении, фруктовых, овощных, рыбных и мясных изделий, маргаринов, безалкогольных напитков, плодово-ягодгых соков.
Регуляторы кислотности:
Лимонная кислота (Е330) —
Выступление на конференции
Л.П.Ходанович
ГБОУ НПО ПЛКМ
14.11.12г.
Все испытал и все проник» — писал о М.В. Ломоносове А.С.Пушкин.
В целях и задачах данной конференции стоит
— воспитание убежденности в возможности познания законов природы и использование достижений науки на благо развития человеческой цивилизации
19 ноября – это день рождения М.В.Ломоносова гениального русского ученого, трудами которого в России был заложен фундамент различных отраслей науки и техники.
Что же он испытал и во что проник – маленький обзор.
М.В. Ломоносов и химия
М.В.Ломоносов жил в эпоху, когда химия только зарождалась как наука и тем не менее он смог наперекор представлениям флогистонской теории дойти до таких обобщений, которые и сегодня лежат в основе физической и химической науки.
М.В. Ломоносов – создатель первой в России химической лаборатории. Ученый имел отчетливое представление о химически чистом веществе и реактиве,
о чем почти не помышляли западные химики и отчего происходила постоянная путаница в опытах.
М.В. Ломоносов был создателем многих химических производств
(неорганических пигментов, глазурей, стекла, фарфора).
Он разработал технологию и рецептуру цветных стекол, которые
употреблял для создания мозаичных картин; изобрел фарфоровую массу.
Он рассмотрел свойства различных металлов, дал их классификацию и
описал способы получения.
Доказывал органическое происхождение нефти, каменного угля, торфа и
янтаря. Им описаны процессы получения железного купороса,
меди из медного купороса, серы из серных руд, квасцов, серной,
азотной и соляной кислот.
Ломоносов обратил внимание на основополагающее значение закона сохранения массы вещества в химических реакциях; изложил основы своего
корпускулярного (атомно-молекулярного) учения, получившего
развитие лишь спустя столетие; выдвинул кинетическую теорию
теплоты; обосновал необходимость привлечения физики для объяснения химических
явлений и предложил для теоретической части химии название “физическая химия”, которая существует и поныне, а для практической части -“техническая химия”.
Ученый создал различные приборы ( прибор для фильтрования под вакуумом,
прибор для определения твердости, газовый барометр, пирометр,
котел для исследования веществ при низком и высоком
давлениях), достаточно точно градуировал термометры.
Одним из конкретных проявлений всеобщего закона природы был открытый и
экспериментально подтвержденный Ломоносовым закон сохранения вещества при химических превращениях, установление которого приписывалось французскому химику Антуану Лорану Лавуазье.
М.В. Ломоносов и физика
Труды Ломоносова в области физики явились крупным вкладом в эту важнейшую науку о природе. Они развивались и дополнялись учеными последующих лет и способствовали тому, что физика стала общепризнанным лидером естествознания.
Ломоносов в астрономии открыл атмосферу Венеры и этот приоритет открытия никем не оспаривается
В области геологии и минералогии была четко сформулирована теория эволюции, лежащая в основе всех явлений природы. Ломоносов изучал причины и природные последствия сейсмических катастроф. Ломоносов ввел в русский язык такие слова, как атмосфера, горный хребет, земная ось, удельный вес и др.
Он подготовил и отредактировал Минеральный каталог Кунсткамеры Академии наук, который был опубликован в 1745году и содержал более трех тысяч образцов руд и минералов.
Один из минералов, найденный в горной породе российские ученые назвали в честь своего великого предшественника ломоносовитом
Ломоносов увлекался и изучал математику, ботанику, историю России, произвел реформу в области русского языка и литературы, утвердил систему русского стихосложения
Во второй половине 18 века русскими мореплавателями была предпринята попытка проникнуть вглубь Северного Ледовитого океана, достичь полюса и пройти в Тихий океан. Эта экспедиция была организована по инициативе М.В.Ломоносова, который, основываясь на опыте русских поморов, пришел к выводу о возможности плавания Северным морским путем .
Еще одно открытие: изучая процесс образования морского льда в «Сибирском океане» , Ломоносов установил, что температура замерзания морской воды зависит от ее солености.
М.В.Ломоносов приложил немало сил и в создании картографии России. Научное картографирование в России связано с деятельностью Географического депортамента
Академии Наук, который в 1758г. возглавил М.В.Ломоносов. Он собрал сведения о природе и экономике губерний, провинций, каждого поселения.
Всего Географический департамент изготовил свыше 250 карт и планов.
Ломоносов – художник и химик — он обратил внимание на мозаику- древнее искусство составлять из цветных стеклянных сплавов (смальт) немеркнущие картины и портреты.
Эпиграфом ко второй части своего выступления я взяла выражение М.В.Ломоносова
«Широко распростирает химия
руки свои в дела человеческие»
М.В. Ломоносов
Следующая задача нашей конференции – применение научных знаний в приобретаемой профессии. А наши профессии – это повар-кондитер.
И сегодня мы остановимся на Пищевых добавках.
В нашей стране список разрешенных пищевых добавок значительно меньше чем за рубежом. Индекс Е специалисты отождествляют как
со словом «Европа» так и со словом «Съедобный»
Присвоение конкретному веществу статуса пищевой добавки и трехзначного номера с индексом «Е» подразумевает, что данное вещество проверено на безопасность.
Однако всегда есть риск, что некоторые люди, например астматики, аллергики и маленькие дети, могут пострадать от пищи, содержащей пищевые добавки.
Согласно Европейской цифровой классификации пищевые добавки подразделяются следующим образом:
Е100 – Е182 — красители (усиливают или восстанавливают цвет продукта);
Е200 – Е299 — консерванты (повышают срок хранения продуктов, защищая от микробов и грибков; химические стерилизующие добавки при созревании вин);
Е300 — Е399 — антиокислители (защищают пищевые продукты от окисления, например жиры от прогоркания, и изменения цвета)
Е400 – Е499 — эмульгаторы (создают однородную смесь несмешиваемых составных частей пищи. Например воды и масла)
Е500 – Е599 — регуляторы кислотности
Е600 – Е699 — усилители вкуса и аромата
Е700 – Е800 — запасные индексы для другой информации
Е900 – и далее – улучшители вкуса хлеба, пеногасители, предупреждают или снижают образование пены в некоторых продуктах питания.
Консерванты – это вещества, которые добавляются в пищевые продукты для максимального их сохранения, предотвращения их порчи.
они не должны иметь токсических и экологических последствий.
К консервантам относятся:
Бензойная кислота (Е210) входит в состав некоторых ягод – брусники, клюквы и является распространенным природным консервантом.
Пропионовая кислота (Е280) и ее соли
Чаще применяют сорбиновую кислоту (Е200) и ее соли
Регуляторы кислотности:
Лимонная кислота (Е330) — широко распространена
в растительном мире.
В нашей стране ее получают из свекловичной мелассы
(отход свеклосахарного производства).
Новое сырье для биотехнического производства лимонной кислоты –
это углеводороды нефти, главным образом жидкие парафины.
— Яблочная кислота (Е296) – природная находится в недозрелой рябине,
яблоках, виноградном соке, ягодах барбариса и малины.
Синтетическая яблочная кислота, полученная из фенола,
не отличается оптической чистотой,
поэтому ее использование как пищевой добавки составляет не более 12%
Антиокислители — вводятся в пищевые продукты для
продления сроков их хранения, предохраняют фрукты, овощи и продукты
их переработки от потемнения при замораживании, консервировании и расфасовке.
В качестве антиокислителя чаще используют чаще
— Аскорбиновую кислоту
Ароматизаторы – усилители вкуса и запаха.
В пищу часто добавляют искусственные усилители вкуса и запаха.
— Глутаминовая кислота (Е620) и ее соли
применяются как пищевая добавка при производстве
маргаринов, бульонных кубиков, соевого мяса и др.
При производстве детских продуктов питания.
В японских ресторанах на столах, наряду с солью и перцем,
обязательно присутствует глутамат натрия.
Подсластители как пищевые добавки
С сахаром человек познакомился около 2500 лет назад,
когда стал получать сахар из тростника.
Существуют еще немало веществ со сладким вкусом –
это неорганические соли бериллия, «свинцовый сахар» или ацетат свинца(11),
соли серебра и др. но многие, из которых ядовиты.
— Сахар иногда называют «белая смерть».
Он является причиной многих заболеваний ожирение , сахарный диабет и др.
связанных с чрезмерным пристрастием к сладкому.
Однако до настоящего времени не найдено подслащивающее вещество,
которое отличалось бы низкой калорийностью, но высокой степенью сладости,
было бы хорошо растворимо, но не было токсичным и не вызывало кариеса.
Есть и сахорозаменители, полученные химическим путем, но они могут
оказывать вредное воздействие на организм человека, особенно детей.
В Японии запрещено применение синтетических сахорозаменителей.
К природным подсластителям относятся:
— Глюкоза (виноградный сахар)
— Лактоза (молочный сахар)
— Фруктоза.
— Сорбит (Е420)
— Ксилит (Е967
— Тауматин (Е957) – белок, выделенный из африканских экзотических
плодов растения Слаще сахара в 4000 раз.
Маленький кусочек тауматина может заменить мешок сахара.
Определяющим фактором сладкого вкуса является
четвертичная структура белка.
Список разрешенных к применению для производства пищевых продуктов
или продажи населению пищевых добавок постоянно пересматривается и обновляется в связи с получением новых данных об их свойствах, внедрении новых препаратов.
Презентация на тему: » «Широко распростирает химия руки свои в дела человеческие… Куда не посмотрим, куда не оглянемся, везде обращаются пред очами нашими успехи ее прилежания»» — Транскрипт:
1
«Широко распростирает химия руки свои в дела человеческие… Куда не посмотрим, куда не оглянемся, везде обращаются пред очами нашими успехи ее прилежания» М. В. Ломоносов
2
Химия — это наука, которая существовала уже за 3-4 тыс. лет до нашей эры
3
Греческий философ Демокрит (V в. до н.э.) Все тела состоят из мельчайших, невидимых, неделимых и вечно движущихся частиц- АТОМОВ Греческий философ Аристотель (IV в. до н. э. ) … в основе окружающей природы лежит вечная ПЕРВОМАТЕРИЯ
4
Древние ремёсла Гончарство Эксперименты с огнём Медицина Металлургия Косметика Стеклоделие
5
Родиной понятия «химия» считают Древний Египет. Происходит от старинного наименования Египта Хемия (греч. Chemía), которое производится от «хем» или «хаме» чёрный и означает «наука чёрной земли» (Египта), «египетская наука». Химические знания тщательно скрывались жрецами. К европейцам химическая наука попала главным образом от арабов после завоевания ими Испании в 711 году. Они называли эту науку «алхимией», от них это название распространилось и в Европе Приставка «ал» – назвала химию «священной наукой»
6
Цель философский камень Удлинить жизнь Исцелить болезни БЕССМЕРТИЕ
7
Изготовление стекла и зеркал Изготовление фарфора Открытие фосфора Г. Брандтом Получены различные элементы в чистом виде
8
М. В. Ломоносов Он создал первый университет. Он лучше сказать, сам был первым нашим университетом. А.С. Пушкин В 1748 г. сформулировал важнейший закон химии – закон сохранения массы вещества в химических реакциях
9
А. М. Бутлеров химик органик В 1861 г создал – теорию строения органических веществ
10
Д. И. Менделеев В 1869 г. открыл основополагающий закон химии – Периодический закон